Forskning & utveckling
Xintela utvecklar med hjälp av sin teknologiplattform nya behandlingsmetoder inom stamcellsterapi och riktad cancerterapi, med fokus på sjukdomsområden där behovet av nya och bättre behandlingsmetoder är mycket stort.
Markörteknologi
Integriner är en familj av cellyteproteiner som reglerar viktiga cellfunktioner och vissa integriner har länge använts som målmolekyler i utveckling av terapier för exempelvis inflammatoriska sjukdomar och cancer. I Xintelas forskning och utveckling används integrin α10β1 som upptäcktes av Evy Lundgren-Åkerlunds forskargrupp vid Lunds universitet. Lundgren-Åkerlund och medarbetare har visat att integrin α10β1 finns på broskceller och på mesenkymala stamceller (MSC) som kan utvecklas till olika celltyper inklusive broskceller. Denna upptäckt ligger till grund för Xintelas process för integrin a10b1-selektion av MSCer och utveckling av stamcellsprodukterna XSTEM® och EQSTEM®.
Stamcellsterapier
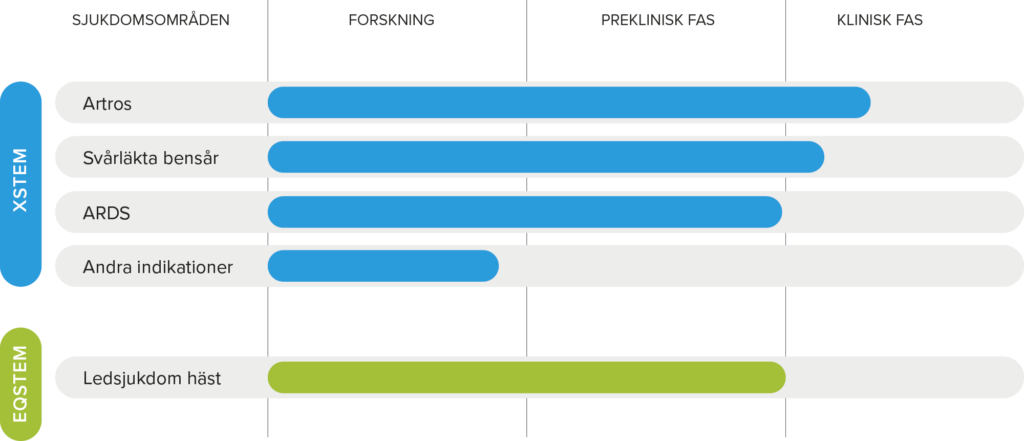
Inom stamcellsterapi används stamcellsmarkören integrin α10β1 för att selektera och kvalitetssäkra stamceller i de patentskyddade stamcellsprodukterna XSTEM®, för behandling av människor, och EQSTEM®, för behandling av hästar. Xintela har framgångsrikt genomfört kliniska studier (fas I/IIa) med XSTEM® för behandling av knäartros och svårläkta venösa bensår och prekliniska studier för behandling av ARDS (Acute Respiratory Distress Syndrome, andnödssyndrom på svenska) samt prekliniska studier med EQSTEM® på hästar med artros.
XSTEM®
Stamcellsprodukten XSTEM®
XSTEM® består av allogena (donerade) integrin α10β1-selekterade och kvalitetssäkrade mesenkymala stamceller (MSCer) från fettväv från friska vuxna donatorer. XSTEM® är patentskyddad både som produkt och för terapeutisk användning inom alla indikationer. Detta ger Xintela en unik position att utveckla säkra och effektiva stamcellsbaserade behandlingar för ett stort antal sjukdomar som idag saknar effektiv behandling.
Egen GMP anläggning
Xintelas stamcellsprodukter produceras i den egna GMP-godkända anläggningen vilket betydligt minskar både produktionskostnader och risker kapacitets- och schemaläggningsrisker i samband med utkontraktering.
Klinisk studie med XSTEM® för behandling av knäartros
Xintela har rapporterat utmärkta 24-månaders resultat från vår avslutade kliniska fas I/IIa studien på knäartros där tre olika dosnivåer av XSTEM® (4, 8 och 16 miljoner stamceller) på totalt 24 patienter (8 patienter/dosnivå) har utvärderats. Resultaten visar att XSTEM® är säker samt att behandlingen ger en signifikant och klinisk relevant minskning av knäsmärta och förbättrad ledfunktion samt förbättrad brosk- och benstruktur vilket bekräftar en långvarig behandlingseffekt och att XSTEM® har sjukdomsmodifierande potential.
Länk till pressmeddelande om studieresultaten »
Läs mer om artros » nedan.
Klinisk studie med XSTEM® för behandling av svårläkta venösa bensår
I Xintelas kliniska studie (fas I/IIa) på patienter med svårläkta venösa bensår har sex patienter har får en behandling av XSTEM® eller placebo applicerat på såret och följts veckovis under tio veckor samt vid fyra månader efter dosering. Det primära målet med studien är att visa att behandlingen är säker och tolererbar. En slutrapport från studien kommer att publiceras i maj 2026.
Läs mer om svårläkta bensår » nedan.
XSTEM® för behandling av Acute Respiratory Distress Syndrome (ARDS)
Xintela har framgångsrikt genomfört prekliniska studier för behandling av ARDS med XSTEM® i samarbete med Skånes Universitetssjukhus. Resultaten visade att XSTEM® minskade blodkagulationen och skador på lungvävnaden. Dessa resultat kan så småningom få tillämpning vid till exempel sepsis där cirka 30 % av patienterna utvecklar ARDS med hög dödlighet.
EQSTEM®
EQSTEM® för ledsjukdom hos hästar
Baserat på bolagets unika teknologi för stamcellsselektion har Xintela utvecklat stamcellsprodukten EQSTEM® för behandling av hästar. EQSTEM® har visat säkerhet och effekt i två prekliniska artrosstudier på hästar. Xintela har ingått ett samarbets- och licensavtal med EQGen Biomedical Inc. för fortsatt utveckling och kommersialisering av EQSTEM® och stamceller för andra djur.
Länk till pressmeddelande »
Länk till publikation (Delco) »
Länk till publikation (Andersen) »
Riktad cancerterapi
Integrin α10β1 – Målmolekyl på aggresiva cancerceller
Xintelas forskning har upptäckt att integrin α10β1 uttrycks på aggressiva och svårbehandlade cancerformer som trippelnegativ bröstcancer, glioblastom och lungcancer. Detta har lett till Xintelas satsning på utveckling av terapeutiska antikroppar och ADCer (antibody drug conjugates) riktade mot integrin α10β1. Vår onkologiverksamhet drivs av vårt helägda dotterbolaget Targinta.
Sjukdomsområden
Artros
Artros är en ledsjukdom som karakteriseras av nedbrytning ledbrosket och försämrad funktion av ledens broskceller. Det är den vanligaste kroniska ledsjukdomen, i synnerhet i knä, höfter och händer, samt den vanligaste orsaken till funktionsnedsättning hos äldre. De främsta symtomen är svår smärta, inflammation, stelhet i leden och nedsatt rörelseförmåga. Sjukdomen drabbar 25 procent av alla individer över 60 års ålder och ökar i omfattning pga en ökande äldre befolkning. Läkemedel som erbjuds idag är framförallt smärtstillande och inflammationsdämpande, vilka behandlar symptomen men inte själva orsaken till ledbroskskadan.
Svårläkta bensår
Svårläkta sår hos äldre, inklusive venösa bensår, är ett stort problem som resulterar i smärta och nedsatt livskvalitet för patienten, samt stora kostnader för hälso- och sjukvården för behandling. Det uppskattas att mellan 0,18 och 1 procent av befolkningen är drabbad venösa bensår. Förekomsten ökar med åldern och uppskattas ligga kring 4 procent bland personer över 65 år. Behandlingar mot svårläkta bensår omfattar kompressionstekniker och en rad olika kirurgiska tekniker, men det saknas helt effektiva läkemedel.
Acute Respiratory Distress Syndrome (ARDS)
ARDS, andnödssyndrom, är en form av akut svår lungsvikt som kan uppstå till följd av exempelvis lunginflammation, trauma och blodförgiftning. Tillståndet innebär att lungornas funktion kollapsar och dödligheten är hög. Det finns idag ingen effektiv behandling av ARDS.
Publikationer
Camper, L., Holmvall, K., Wängnerud, C., Aszódi, A., and Lundgren-Åkerlund, E. ”Distribution of the collagen-binding integrin α10β1 during mouse development.” Cell Tissue Res. 306, 107-116 (2001).
Bengtsson, T., Camper, L., Schneller, M., and Lundgren-Åkerlund, E. ”Characterization of the mouse integrin subunit α10 gene and comparison with its human homologue. Genomic structure, chromosomal localization and identification of splice variants.” Matrix Biology 20, 565–76 (2001).
Camper, L., Hellman, U., and Lundgren-Åkerlund, E. Isolation, ”Cloning, and Sequence Analysis of the Integrin Subunit α10, a β1-associated Collagen Binding Integrin Expressed on Chondrocytes.” Journal of Biological Chemistry 273, 20383–20389 (1998).
Bengtsson, T., Aszódi. A., Nicolae, C., Hunziker, E.B., Lundgren-Åkerlund, E. and Fässler, R. ”Loss of α10β1 integrin expression leads to moderate dysfunction of growth plate chondrocytes. ” Journal of Cell Science 118, 929–36 (2005).
Varas, L., Bryngelson Ohlsson, L., Honeth, G., Olsson, A., Bengtsson, T., Wiberg, C., Bockermann, R., Järnum, S., Richter, J., Pennigton, D., Johnstone, B. Lundgren-Åkerlund, E and Kjellman, C. ”α10 Integrin expression is up-regulated on fibroblast growth factor-2-treated mesenchymal stem cells with improved chondrogenic differentiation potential. ” Stem Cells and Development 16, 965–978 (2007).
Lundgren-Åkerlund E., Aszòdi A. ”Integrin α10β1: a collagen receptor critical in skeletal development” Adv
Exp Med Biol. 819:61-71. (2014)
Zeltz C, Lu N, Gullberg D. “Integrin α11β1: a major collagen receptor on fibroblastic cells” Adv Exp Med Biol. 819:73-83. (2014)
Munksgaard Thorén M., Chmielarska Masoumi K., Krona C., Huang X., Kundu S., Schmidt L., Forsberg-Nilsson K., Floyd Keep M., Englund E., Nelander S., Holmqvist B. and Lundgren-Åkerlund E. “Integrinα10,a Novel Therapeutic Target in Glioblastoma, Regulates Cell Migration,Proliferation, and Survival.” Cancers (Basel). 11, 587 (2019).
Uvebrant K., Reimer Rasmusson L., Talts JF., Alberton P., Aszodi A., and Lundgren-Åkerlund E. “Integrinα10β1-selected Equine MSCs have Improved Chondrogenic Differentiation, Immunomodulatory and Cartilage Adhesion Capacity.” Ann Stem Cell Res. 2,001–009 (2019).
Delco ML., Goodale M., Talts JF.,Pownder SL., Koff MF., Miller AD., Nixon B., Bonassar LJ., Lundgren-Åkerlund E., and Fortier LA. “Integrin α10β1-SelectedMesenchymal Stem Cells Mitigate the Progression of Osteoarthritis in an EquineTalar Impact Model.” Am J Sports Med. 48, 612-623 (2020).
Andersen, C., Uvebrant, K., Mori, Y. Aarsvold S., Jacobsen S., Berg LC., Lundgren Åkerlund, E., and Lindegaard C. ”Human integrin α10β1-selected mesenchymal stem cells home to cartilage defects in the rabbit knee and assume a chondrocyte-like phenotype.” Stem Cell Res Ther. 13, 206 (2022).
Clarke EJ., Johnson E., Caamano Gutierrez E., Andersen C, Berg LC., Jenkins RE., Lindegaard C., Uvebrant K., Lundgren-Åkerlund E., Turlo A., James V., Jacobsen S., and Peffers MJ. “Temporal extracellular vesicle protein changes following intraarticular treatment with integrin α10β1-selected mesenchymal stem cells in equine osteoarthritis.” Front Vet Sci. 9:1057667 (2022).
Edström D., Niroomand A., Stenlo M., Uvebrant K., Bölükbas DA., Hirdman G., Broberg E., Lim HC., Hyllén S., Lundgren-Åkerlund E., Pierre L., Olm F., Lindstedt S. ”Integrin α10β1-selected mesenchymal stem cells reduced hypercoagulopathy in a porcine model of acute respiratory distress syndrome.” Respir Res. 24(1):145 (2023).
Andersen C., Jacobsen S., Uvebrant K, Griffin, IV, JF., Vonk LA., Walters M., Berg LC., Lundgren-Åkerlund E., and Lindegaard C. ”Integrinα10β1-Selected Mesenchymal Stem Cells ReducePain and Cartilage Degradation and Increase Immunomodulation in an EquineOsteoarthritis Model.” Cartilage. doi: 10.1177/19476035231209402 (2023).
Andersen C., Walters M., Bundgaard L., Berg LC., Vonk LA., Lundgren-Åkerlund E., Lyngfeldt Henriksen B., Lindegaard C., Skovgaard K., and Jacobsen S. “Intraarticular treatment with integrin α10β1-selected mesenchymal stem cells affects microRNA expression in experimental post-traumatic osteoarthritis in horses.” Front Vet Sci. 11:1374681 (2024).